斯克裡普斯研究所的科學傢們發現一個關鍵特性,這是CELMoD--一類有前途的新癌癥藥物有效發揮作用所必需的。CELMoDs是一類新的癌癥藥物,其功能是與cereblon(一種調節蛋白)結合,導致驅動癌癥的蛋白質降解。研究人員發現,CELMoDs要有效地發揮作用,它們必須在結合後引起cereblon的特定形狀變化。
最近發表在《科學》雜志上的這一發現使人們能夠可靠地設計出有效的CELMoDs。
研究報告高級作者、斯克裡普斯研究中心綜合結構和計算生物學系教授Gabriel Lander博士說:"有很多研究小組花相當多的時間制造與腦蛋白結合得非常緊密的藥物,但隨後又不解地撓頭,因為這些藥物未能發揮作用。"該研究的第一作者是蘭德爾實驗室的博士後研究員Randy Watson博士。
Cereblon作為細胞中一個主要的蛋白質處置系統的一部分發揮作用。這個系統用稱為泛素的分子來標記目標蛋白,而泛素標記的蛋白會被稱為蛋白酶體的遊動蛋白分解復合體破壞。泛素-蛋白酶體系統不僅用於破壞異常或受損的蛋白質,而且還用於幫助調節一些正常蛋白質的水平。Cereblon是泛素-蛋白酶體系統使用的數百種"適配器"之一,用於引導泛素標記過程向特定的目標蛋白集發展。
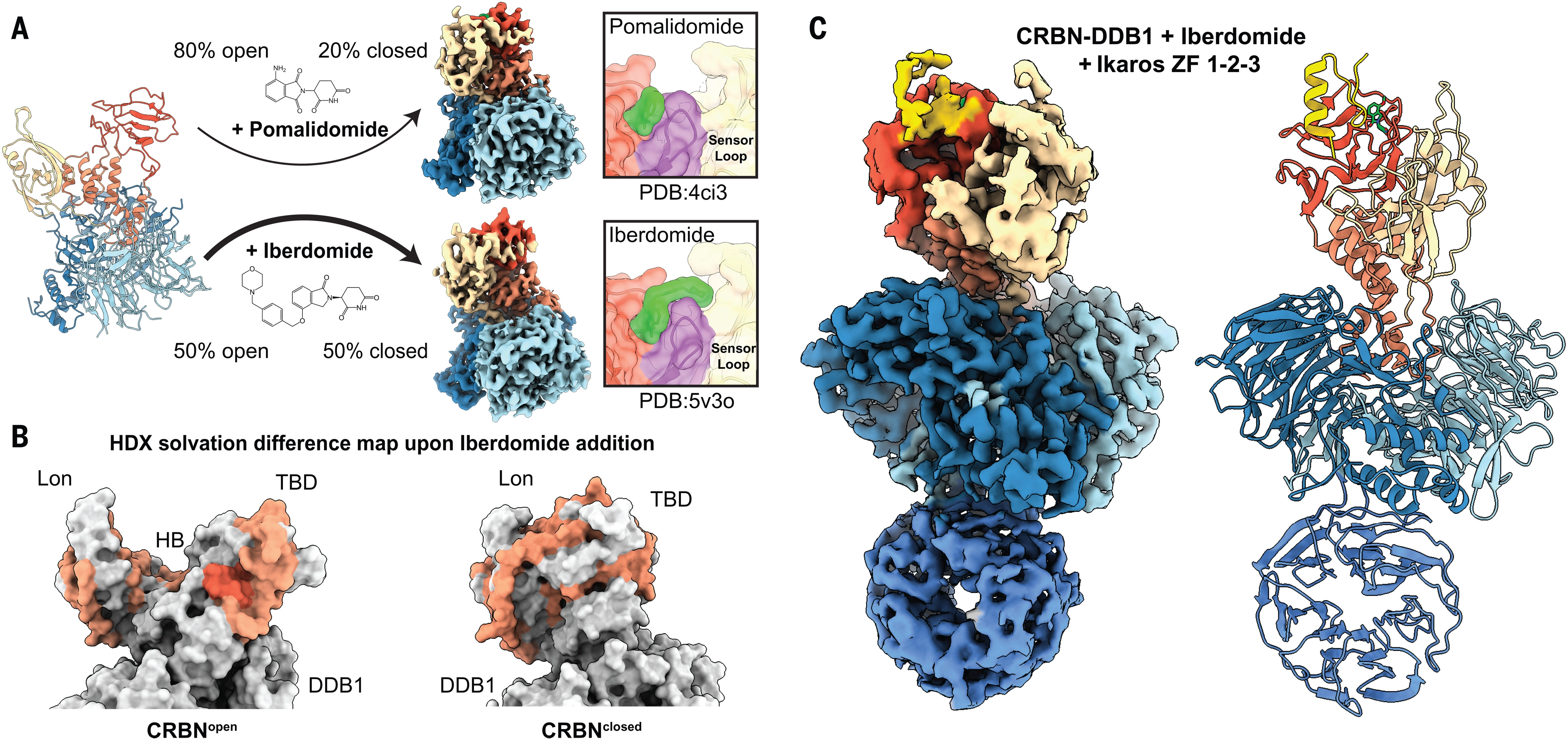
科學傢們現在認識到,一些癌癥藥物,包括最暢銷的骨髓瘤藥物來那度胺(Revlimid)恰好通過與cereblon結合發揮作用。他們這樣做是為迫使泛素標記,以及隨之而來的對促進細胞分裂的關鍵蛋白的破壞--這些蛋白不容易被傳統藥物作為目標。部分受到這種認識的啟發,藥物公司已經開始開發腦蛋白結合藥物-CELMoD,也被稱為蛋白質降解藥物,被證明對骨髓瘤和其他癌癥的治療效果更好。

這一發現將幫助藥物開發商創造出更有效的CELMoD,它在治療廣泛的嚴重疾病--包括癌癥--方面顯示出前景。
該領域的一個持久問題是,這些藥物中的一些與腦蛋白緊密結合,但卻不能導致其蛋白質目標的充分降解。解為什麼會發生這種情況一直很困難。科學傢們希望使用高分辨率的成像方法來繪制cereblon的原子結構圖,並研究其與CELMoDs結合時的動態變化。但腦蛋白是一種相對脆弱的蛋白質,很難用這種成像方法來捕捉。
在這項研究中,Watson花一年多的時間設計一個穩定cereblon與泛素系統夥伴蛋白的配方,以便用低溫電子顯微鏡(cryo-EM)對其成像。通過這種方式,他最終能夠在近原子尺度上解決腦蛋白的結構。Watson還對有CELMoD化合物和目標蛋白的cereblon-夥伴復合物進行成像。
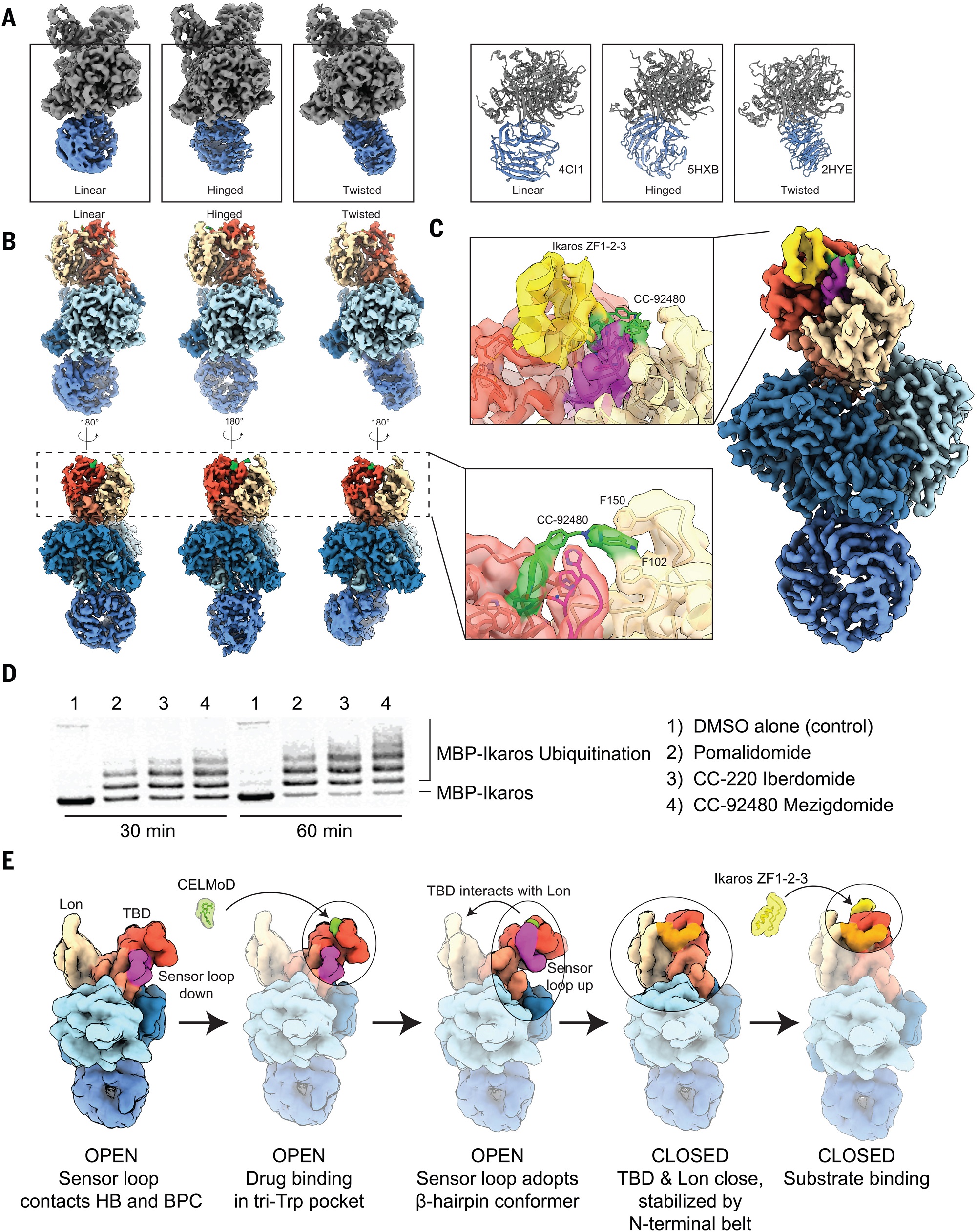
結構數據顯示,CELMoD必須以改變其形狀或構象的方式與cereblon結合。研究人員確定,Cereblon有一個默認的"開放"構象,但必須切換到一個特定的"封閉"構象,以便對目標蛋白進行泛素標記。這一發現的主要意義在於,開發CELMoD的藥物公司現在對他們的候選藥物必須做什麼才能有效有更好的認識。
"公司一直在開發腦結合蛋白降解藥物,他們可以看到這些藥物是更好的降解劑,但他們不知道這是因為這些藥物能更好地驅動這種封閉構象,"Watson說。"所以現在他們知道,他們可以測試他們的藥物的這一關鍵特性。"
Watson用於穩定腦蛋白以準備低溫電鏡成像的突破性配方現在也被該領域的研究人員廣泛采用。
Lander說,他的實驗室現在希望能促進蛋白質降解藥物的開發,這些藥物通過與除cereblon之外的其他泛素-蛋白酶體適應蛋白結合而發揮作用。正如他所指出的,蛋白降解藥物策略的最大吸引力在於它可以用來打擊幾乎所有與疾病有關的蛋白質,包括傳統藥物無法瞄準的一大類蛋白質