2月7日,英國權威醫學雜志《自然》發佈題為《新冠藥物刺激病毒突變——現在有人想停止使用它(COVIDdrugdrivesviralmutations—andnowsomewanttohaltitsuse)》的文章稱,一項對1300多萬個SARS-CoV-2(新冠病毒)序列進行調查的研究發現,莫諾拉韋膠囊(Molnupiravir,商品名:利卓瑞®/LAGEVRIO®)的治療引發攜帶大量突變的病毒
對此,莫諾拉韋藥物生產商、美國制藥公司默沙東(Merck & Co.)2月9日回復媒體稱,“文章作者推測這些變異與莫諾拉韋的使用有關,其推論僅建立在病毒序列的來源和時間范圍與該地區莫諾拉韋是否可及的間接關聯,然而並無直接證據證明這些病毒基因序列來自於經莫諾拉韋治療的患者。多項臨床試驗數據顯示莫諾拉韋能夠使病毒感染(率)快速降低。”
藥物刺激變異?默沙東回應
據《自然》雜志,該研究於2023年1月27日發表於論文預印本平臺medRxiv上,目前還未經同行評審。彭博社報道中稱,在新冠病毒大流行期間,科學傢們越來越多地開始在全面的“同行評審”之前,在所謂的預印本上發表他們的研究,以更快地推進研究、分享他們的成果。
《自然》雜志文章稱,科學傢們提出一種可能性,稱在極少數情況下,莫諾拉韋的治療可能無法完全消除新冠病毒,且使得一些服用該藥物的人繼續傳播病毒。此外,研究人員對全球序列的分析表明,2022年,也就是莫諾拉韋被廣泛使用的第一年,可疑病毒譜系的患病率出現大幅上升,而且這類病毒也更有可能出現在莫那匹韋已經獲批的國傢(例如美國、英國和澳大利亞)。

圖片來源:《自然》雜志
莫諾拉韋由美國制藥巨頭默沙東公司開發,於2021年底獲得美國和英國的批準上市,並於次年在澳大利亞獲批。2022年12月30日,莫諾拉韋在中國國內獲批上市,價格為1500元/盒。
由默沙東公司資助的一項臨床試驗發現,在服用莫那匹韋膠囊5天後,減少新冠重癥病人的住院率和死亡率。另據公開資料,莫諾拉韋是RNA聚合酶抑制劑,可與新冠病毒的RNA聚合酶結合,在新合成的RNA分子中引入錯誤的核苷酸,從而起到抑制或清除病毒的作用。
彭博社報道稱,一些研究人員擔心這種藥物可能會產生更具傳染性或威脅健康的新冠病毒變種。由弗朗西斯克裡克研究所(Francis Crick Institute)、倫敦帝國理工學院和其他英國機構的研究人員發表的該篇文章顯示,從數十名患者身上采集的病毒樣本中,發現與使用默沙東公司莫諾拉韋藥物有關的突變。
報道還稱,其實莫諾拉韋膠囊在2021年晚些時候在美國獲批之前,一些科學傢就警告稱,根據該藥物的工作原理,這種藥物可能會導致基因的突變,最終可能會產生問題。
不過,彭博社同時援引默沙東的發言人稱,“沒有證據表明任何抗病毒藥物導致病毒變體的出現。根據現有數據,我們不認為莫諾拉韋膠囊可能刺激新的新冠病毒變體。”美國食藥監局(FDA)則表示,該機構不對第三方的研究發表評論,隻與新冠病毒制藥商合作評估其產品對病毒變體的活性。
《每日經濟新聞》記者註意到,在medRixv刊登上述文章後,本月初,默沙東就通過美國醫學雜志《貝克爾醫院評論》(Becker‘s Hospital Review)做出回應,稱該研究的證據隻能“間接”將莫諾拉韋與病毒突變聯系起來,沒有直接證據證明這些病毒基因序列來自於經莫諾拉韋治療的患者。
多名研究員建議停用
該文章的作者之一、來自印第安納州的獨立研究員Ryan Hisner表示,藥物相關突變的風險太大,不建議繼續使用默沙東公司的藥物。斯坦福大學抗病毒藥物研究員Michael Lin則認為,美國應該探索授權其他國傢使用的藥物來控制新冠病毒,比如日本鹽野木公司的恩司特韋(Xocova),並停止使用莫諾拉韋膠囊。
《自然》雜志還引用加拿大溫哥華不列顛哥倫比亞大學的進化生物學傢Sarah Otto的觀點稱,(發佈於medRixv的)論文是對莫諾拉韋膠囊的又一次打擊。她指出,另有英國的一項大規模研究表明,該藥物沒有改善住院率或死亡率。“我希望公共衛生相關領導能夠呼籲在全球范圍內停止使用它。”Otto說道。
根據美國國立衛生研究院的說法,一般來說,在有替代藥物的情況下,患者不應服用莫諾拉韋膠囊。
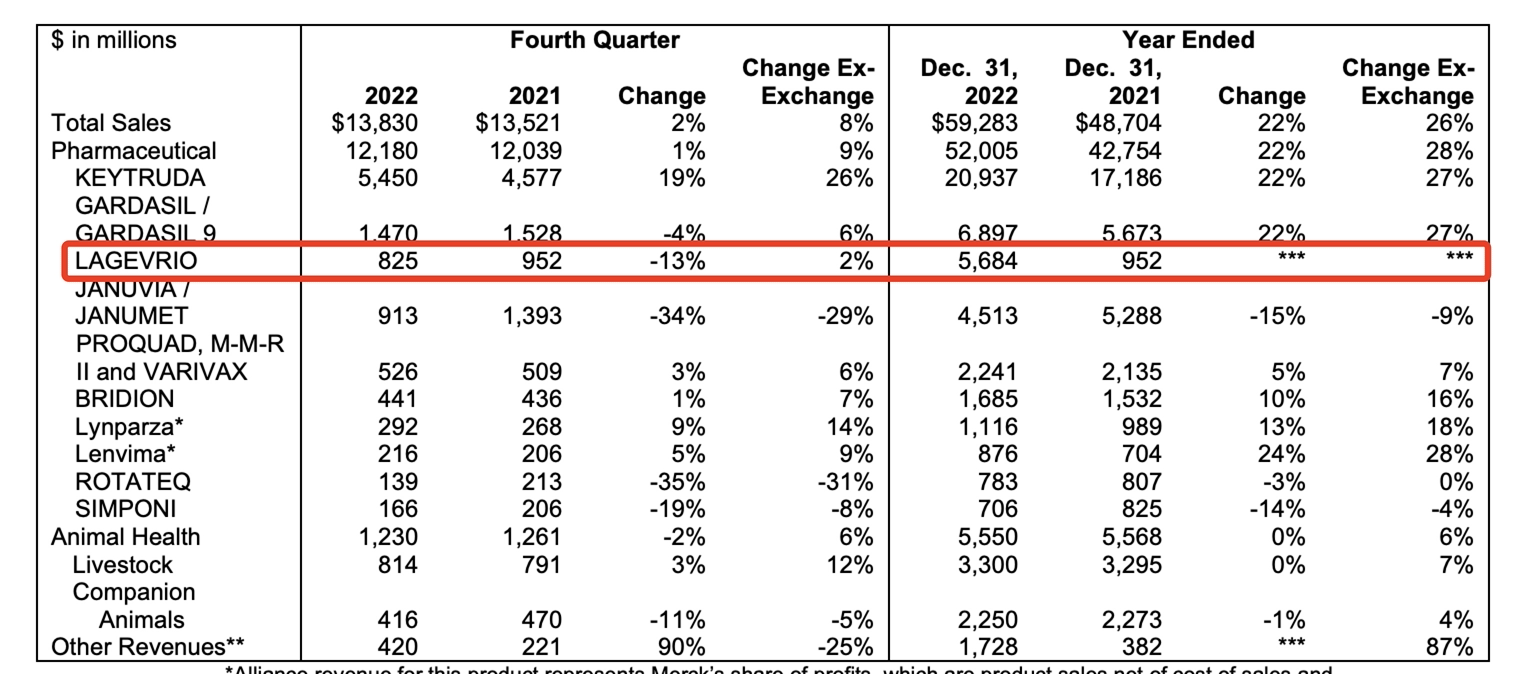
圖片來源:默沙東年報
上周,默沙東發佈2022年全年財報。去年,默沙東全年銷售額為593億美元,同比增長22%,其中莫諾拉韋膠囊全年銷售額為約57億美元。報告期內,默沙東中國全年銷售額為51億美元,同比增長20%。
默沙東預估2023全年銷售額將達572億至578億美元,其中包括約10億美元的莫諾拉韋膠囊銷售額。