9月26日,國傢藥品監督管理局批準上海艾普強粒子設備有限公司生產的“質子治療系統”創新產品註冊申請。該產品是“十三五”期間科技部重點研發計劃“數字診療裝備專項”的重點支持項目,也是我國首臺獲準上市的國產質子治療系統。該產品的獲批上市,標志著我國高端醫療器械裝備國產化又邁出一步,對提升我國醫學腫瘤診療手段和水平,具有重大意義。
9月26日,國傢藥品監督管理局批準上海艾普強粒子設備有限公司生產的“質子治療系統”創新產品註冊申請。 國傢藥品監督管理局官網截圖
該產品由加速器系統和治療系統兩部分組成。其中加速器系統包括註入器系統、低能傳輸系統、主加速器系統、高能束流傳輸系統和輔助電氣系統,治療系統包括固定束治療系統、180°旋轉束治療系統和治療計劃系統。產品提供質子束進行放射治療,在實現腫瘤部位高劑量的同時,可降低周圍正常組織劑量,特別是靶區後組織的劑量,適用於治療全身實體惡性腫瘤和某些良性疾病,具體適應證應由臨床醫師根據實際情況確定。
質子治療是世界上最先進的腫瘤治療手段之一,患者在治療過程中無需開刀,有治療精準、副作用小、患者生活質量高的優點,除常規放療適應證,尤其適合兒童腫瘤等的精準治療。
澎湃新聞曾於2022年4月報道,全球成功運行的質子放療系統主要在美國、歐洲和日本,為滿足國內臨床需求,打破國外質子治療技術壟斷,促進國產質子治療裝置的研發與產業化,由中國科學院上海應用物理研究所、中國科學院上海高等研究院、上海艾普強粒子設備有限公司和上海交通大學醫學院附屬瑞金醫院等聯合研發“國產首臺質子治療系統”,並於2012年正式立項,如今獲批上市可謂“十年磨一劍”。
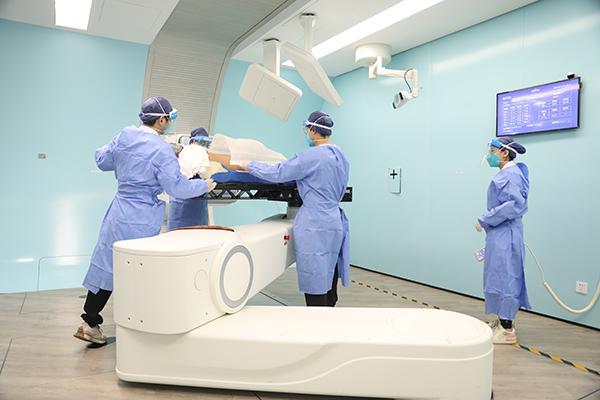
2022年4月26日上午,上海交大醫學院附屬瑞金醫院啟動國內首臺國產質子治療示范裝置180度旋轉束治療,圖為180度旋轉束治療室。瑞金醫院 供圖
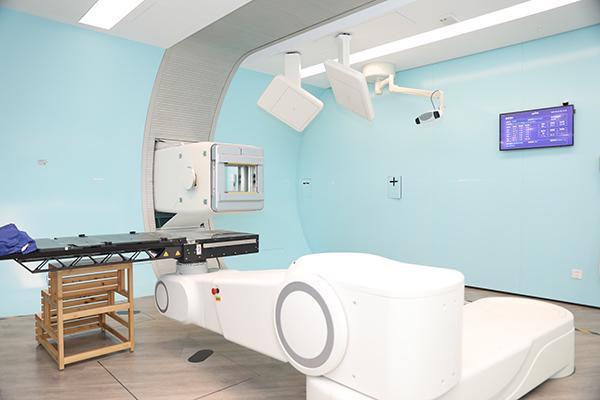
國內首臺國產質子治療示范裝置180度旋轉束治療室。瑞金醫院 供圖
在該產品的註冊申報過程中,國傢藥監局按照“提前介入、專人負責、全程指導,科學審批”的原則,在標準不降低、程序不減少的前提下,積極溝通,多方協調,加大產品註冊申報指導,加快審評審批進程,在保證安全、有效的基礎上推動產品盡快上市,滿足患者使用高水平醫療器械的需要。
而在上海,上海市藥監部門按照“前期介入、專人負責、專業指導”原則,構築全方位服務指導體系,賦能醫療器械創新發展;“優化服務方式、優化服務流程”,有效激發創新產品研發活力,縮短企業品種上市進程;構建全生命周期監管機制,推動產業健康發展。
國傢藥品監督管理局在其官網上發佈提醒,使用者應當嚴格按照產品批準的適用范圍使用產品,同時應當嚴格遵守衛生健康部門的診療規范。