AI,能夠重寫人類基因組?就在剛剛,初創公司Profluent宣佈,完全由AI設計的基因編輯器,已經成功編輯人類細胞中的DNA。也就是說,世界上首個使用AI從頭設計的分子級精確基因編輯器誕生。

就像ChatGPT能生成詩歌一樣,Profluent這個全新的AI系統,可以讓我們編輯自己DNA的微觀機制生成藍圖。
在迄今最廣泛的基於CRISPR的基因編輯系統數據集上,研究者訓練LLM。這些LLM產生的蛋白質,將幾乎所有天然存在的CRISPR-Cas傢族的多樣性,擴大4.8倍!
並且,基因編輯器在人類細胞中顯示出與SpCas9(一個示例基因編輯器)相當或更好的活性和特異性,同時距離超過400個突變。
這也就意味著,我們掌握自己的基因組密碼。未來的科學傢,會比今天更精確、更快速地對抗疾病。
而且,公司還決定,會在OpenCRISPR協議下,自由釋放這些DNA分子。
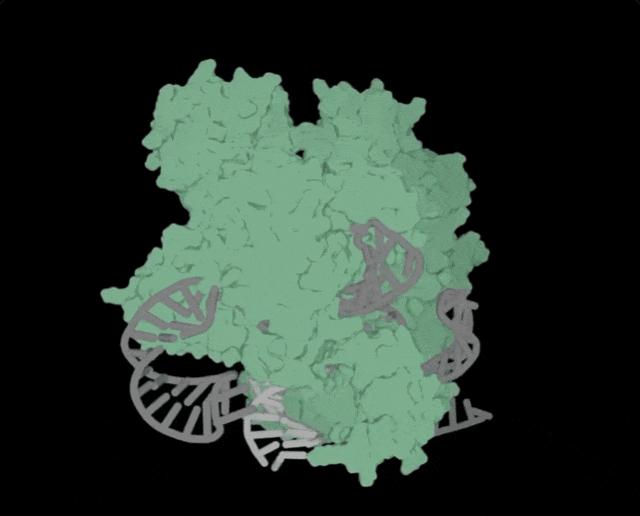
OpenCRISPR-1的物理結構,OpenCRISPR-1即是由Profluent的AI技術創建的基因編輯器
Profluent聯創Ali Madani表示,“嘗試用AI設計的生物系統,編輯人類DNA是一次科學登月之旅”。
“我們的成功表明,在未來,AI可精準設計出一系列定制的疾病治療方案”。
有網友表示,“是時候重新編程人類嗎?AI驅動的CRISPR技術進步,正挑戰著基因倫理的邊界”。

如果你可以改變自己的DNA,你會這麼做嗎?

貧血、失明疾病的基因,由我們自己修改
初創公司Profluent在剛剛發表的這篇論文中,詳細描述這項技術。

論文地址:https://www.biorxiv.org/content/10.1101/2024.04.22.590591v1.full.pdf
論文預計將於下月,在美國基因與細胞治療學會年會上發表。
這項技術和驅動ChatGPT的方法是一樣的,它在分析大量生物數據後,創造新的基因編輯器,包括科學傢已經用於編輯人類DNA的微觀機制。
這些基因編輯器基於的是諾獎的獲獎方法,涉及一種名叫CRISPR的生物機制。

基於CRISPR的技術誕生後,即在業界引起轟動。它改變科學傢研究疾病的方式。
在以前,如果我們不幸得鐮狀細胞性貧血和失明這樣的遺傳性疾病,往往束手無策,而現在,CRISPR技術可以直接讓我們修改導致這些疾病的基因!
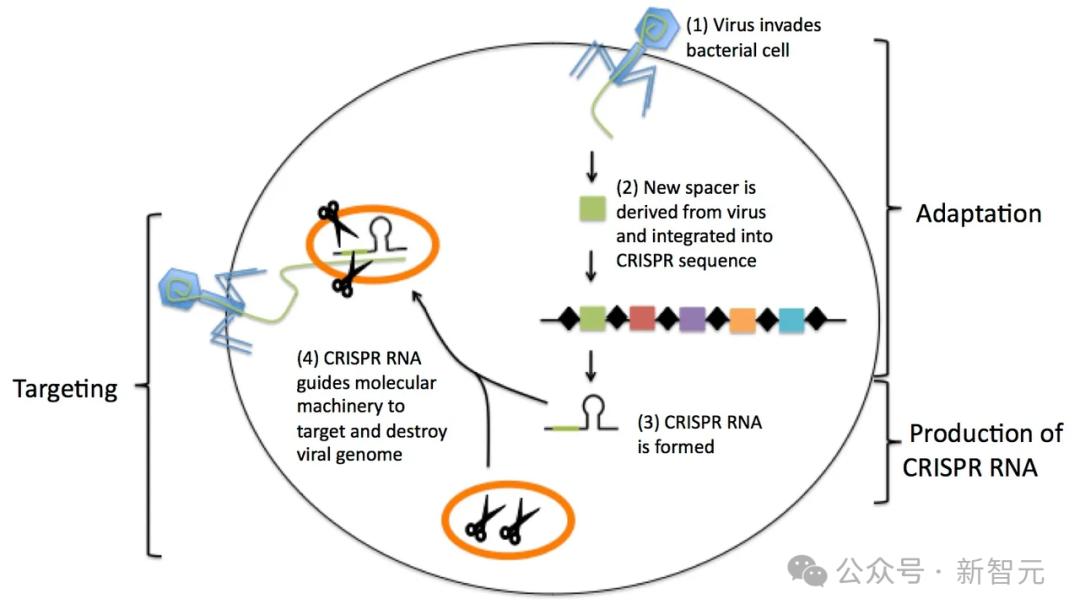
CRISPR方法使用的是我們在自然界中發現的機制:從細菌中收集的生物材料,竟然神奇地賦予這些微生物抵抗細菌的能力。
加州大學舊金山分校生物工程和治療科學系教授兼系主任James Fraser介紹說,這些生物材料從未在地球上存在過,而Profluent的AI系統,正是從大自然中學習如何創造這些全新的東西。
如果這些技術繼續發展,所產生的基因編輯器,或許會比我們人類經過數十億年進化磨練的基因編輯器更靈活、更強大。
現在,Profluent表示正在開源OpenCRISPR-1編輯器,這也就意味著,個人、學術實驗室和公司都能免費使用這些技術。
AI界常見的開源,可以加速新技術的產生。不過,對於生物實驗室和制藥公司來說,像OpenCRISPR-1這樣的開源並不常見。
當然,Profluent也隻是開源其AI技術生成的基因編輯器,並沒有開源AI技術本身。
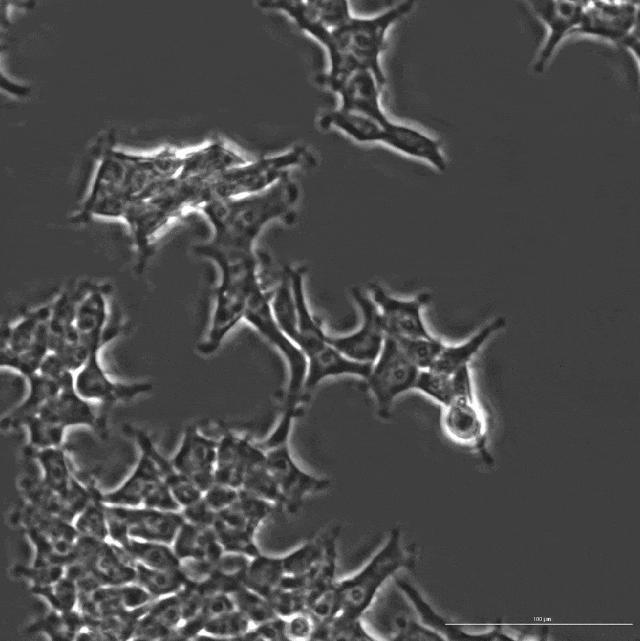
由OpenCRISPR-1編輯的人類細胞延時攝影
AI編輯蛋白質,為何意義重大
目前,蛋白質工程界想要復制功能性蛋白質,或者用“定向進化”來迭代修飾,通常還是需要從自然界中復制。
許多對人類有重大意義的蛋白質,都是我們偶然發現的,比如狗的胰島素、酸奶設施中的Cas9和經常造成食物中毒的肉毒桿菌毒素。
大型生成蛋白質語言模型的作用,就是可以捕獲使天然蛋白質發揮作用的基本藍圖。它們勾勒出一條捷徑,可以繞過進化的隨機過程,推動人類有意識地為特定目的設計蛋白質。
Cas9蛋白,是CRISPR-Cas9基因編輯系統的核心組成部分,它是一種RNA引導的核酸酶,可以搜索人類基因組中的所有30億個核苷酸,並在一個特定位點進行切割。
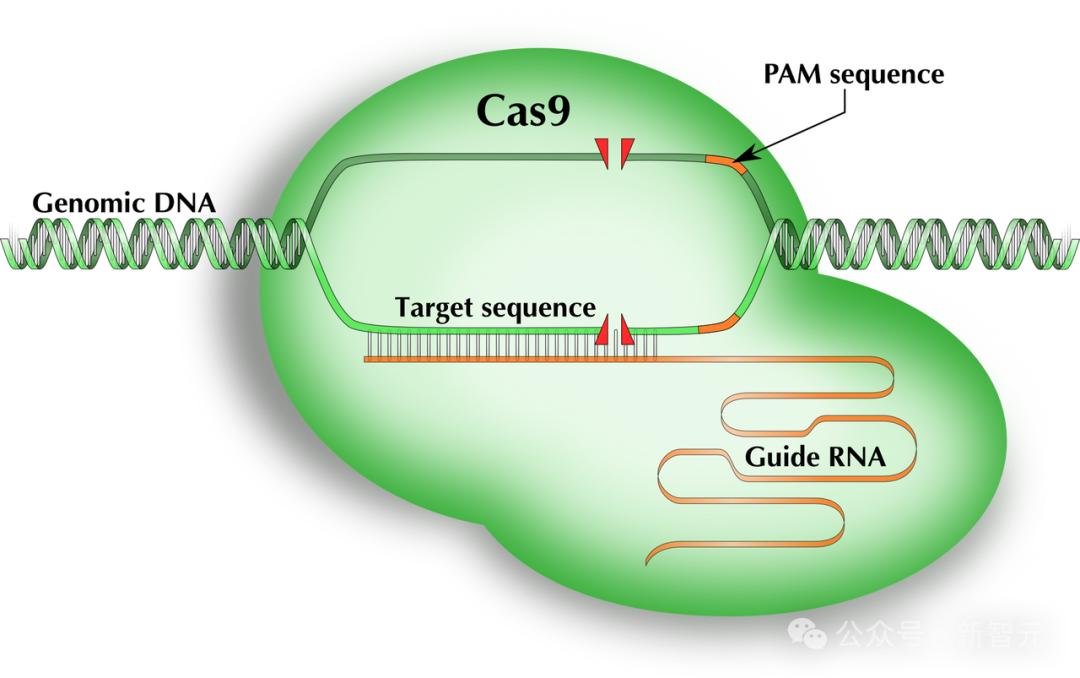
這種核酸酶與單導RNA(sgRNA)復合在一起,sgRNA由一個在結構上與蛋白質相互作用的支架和一個間隔序列組成,後者可通過編程靶向基因組中的任何位點。
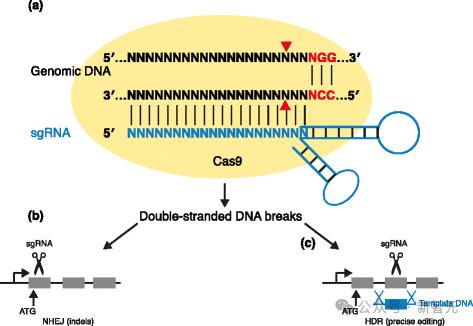
棘手的是,大多數Cas9蛋白的長度超過1000個氨基酸,整個設計空間包含20^1000種可能的序列,比起可觀測宇宙中的原子數量,它都要高出幾個數量級!

而且,由於這些蛋白質必須以精確的順序協調許多相互作用,才能實現精確切割,因此即使是單個錯位突變,也可能完全消除蛋白質的功能。
如果通過實驗窮盡所有可能的序列變異,許多科學傢幾輩子時間都做不完。
然而,AI系統卻能很輕松地探索整個搜索空間,發現功能性的基因編輯器。而且,隻需要花幾個小時!
全球首個開源基因編輯器,改寫人類DNA
基因編輯器OpenCRISPR-1,由一個Cas9樣蛋白質,和引導RNA(guide RNA)構成。
正如之前所述,它是完全由Profluent的AI大模型開發的。
在具體實現過程中,研究人員對26TB組裝的“基因組”和“元基因組”數據庫系統進行挖掘,整理出超100萬個CRISPR操縱子(operon)的數據集。
通過訓練OpenCRISPR,AI從大規模序列和生物背景中學習,生成自然界不存在的數百萬種CRISPR樣蛋白。

研究人員稱,AI生成自然界中已發現的“CRISPR-Cas傢族”的4.8倍的蛋白質集群,完全實現指數級擴展!
而且,語言模型還為類Cas9效應蛋白定制單引導RNA序列。
與原型基因編輯效應器SpCas9相比,幾個生成的基因編輯器顯示出,可比或改進的活性和特異性,同時在序列上相差400個突變。
最後,研究人員還證明AI生成的基因編輯OpenCRISPR-1與堿基編輯的兼容性。
這項研究中的關鍵結果,具體如下。
AI生成4.8倍“CRISPR-Cas”蛋白質宇宙
生成蛋白質語言模型通常是在,大型涵蓋多種系統發育和功能的天然蛋白序列的數據集上,進行預訓練 。
這些模型能夠生成,反映天然蛋白質分佈和特性的真實蛋白質序列。
然而,對於特定的應用,例如新型基因編輯器的生成,有必要將生成過程導向特定的感興趣的蛋白傢族子集。
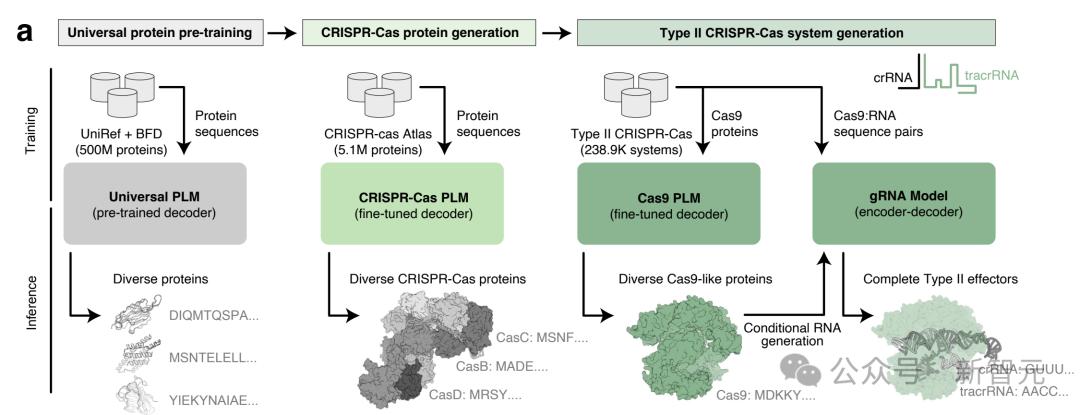
對此,研究人員進行詳盡的數據挖掘來構建數據庫。
他們搜索26.2TB的組裝微生物基因組和宏基因組,發現1,246,163個CRISPR-Cas操縱子。
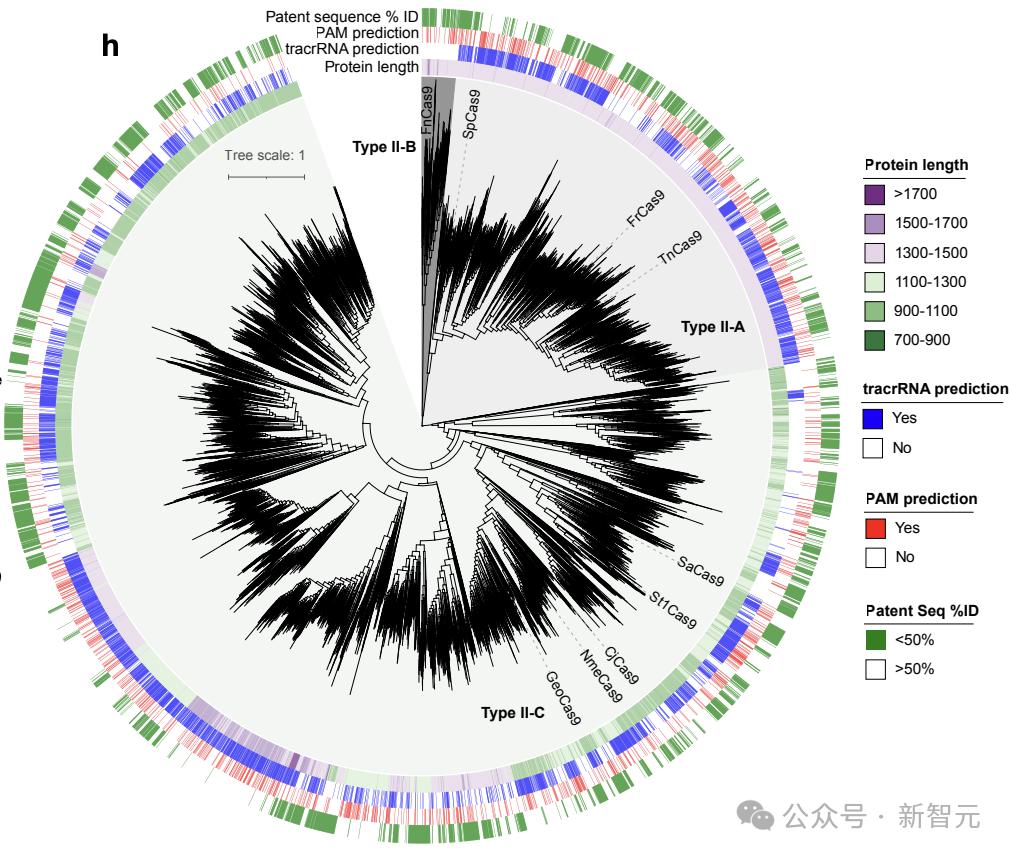
與CRISPRCasDB和CasPDB等精選數據庫,以及世界上最大的蛋白質資源UniProt相比,最新創建的數據庫顯示出更大的多樣性。
通過總結共性,研究人員發現所有CRISPR-Cas蛋白的單一模型,能夠生成跨傢族的不同序列。
為生成新型CRISPR-Cas蛋白,作者在CRISPR-Cas Atlas上微調基於ProGen2的語言模型,由此平衡蛋白傢族的表示和序列簇大小。
從這個模型中,研究者生成400萬個序列。
其中一半是直接從模型生成的,另一半是由天然蛋白質N或C末端的最多50個殘基提示,以引導向特定蛋白的生成。
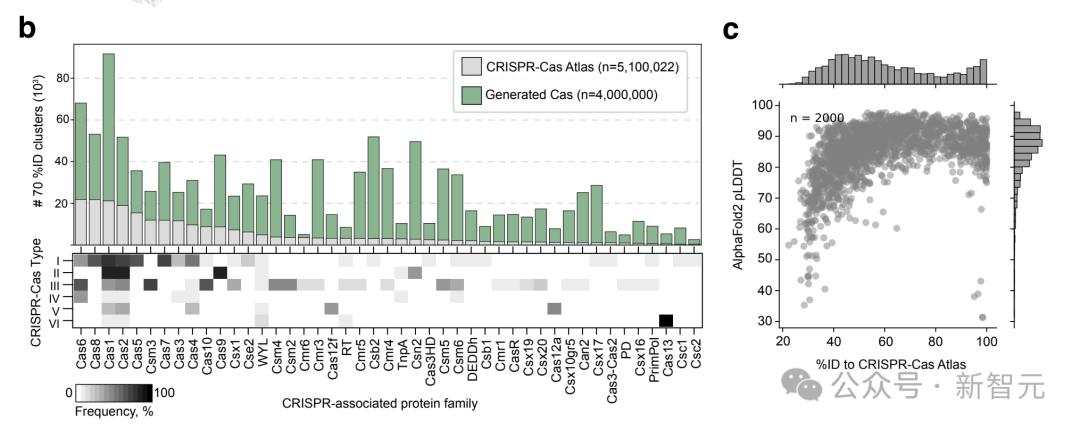
為評估其新穎性和多樣性,作者使用MMseqs2對每個傢族的生成序列和天然序列按70%的同一性進行聚類。
結果發現,與CRISPR-Cas圖譜中的天然蛋白相比,生成序列實現4.8倍的多樣性擴展。
對於天然蛋白質很少的傢族,比如Cas13和Cas12a,生成序列的多樣性分別增加8.4倍和6.2倍。
另外,隻需要極少的上下文,即提供50個或更少的殘基,就能針對某一特定科引導序列生成與感興趣的科保持一致。
100萬個類Cas9蛋白全部生成
雖然許多CRISPR-Cas蛋白已被用於基因組編輯 ,但Cas9仍是應用最廣泛的一種。
為生成類Cas9的新序列,研究人員從CRISPR-Cas圖譜中采樣,Cas9的N端或C端50個殘基,對CRISPR-Cas模型進行提示。
這裡,作者使用CRISPR-Cas Atlas中238917條Cas9序列,對另一個語言模型進行微調。
這一模型生成可行的類Cas9序列的速度是CRISPR-Cas模型的2倍(54.2%),而且需要任何提示。

為探索II型效應器的潛在序列分佈,研究人員使用Cas9模型生成100萬個Cas9蛋白。
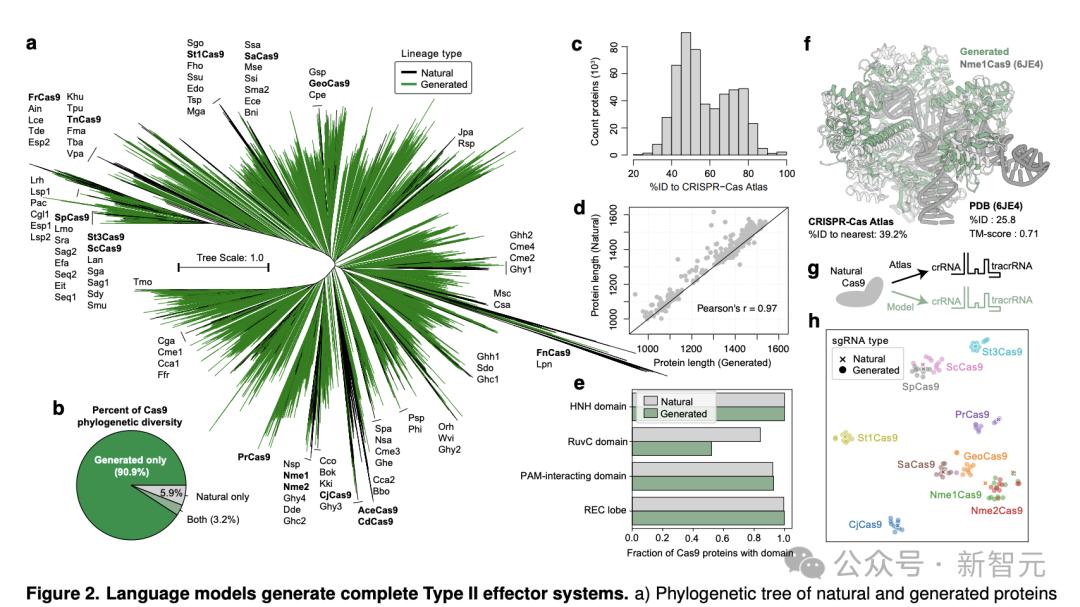
生成的可存活代(n=542,042)與同一性為40%的天然Cas9聚類在一起,並用作構建最大似然系統發育樹的輸入(圖2a)。
引人註目的是,生成的蛋白質主導系統發育的格局,占系統發育總多樣性的94.1%。
與整個CRISPR-Cas圖譜相比,多樣性增加10.3倍(圖2b)。
新的系統發生群分佈在整個樹中,這表明該模型捕捉到Cas9的全部多樣性,並沒有過度擬合任何特定系。
生成的序列與CRISPR-Cas圖譜的差異很大,與任何自然序列的平均同一性隻有56.8%(圖2c)。
總體而言,生成的序列與同一蛋白質簇中天然蛋白質的長度密切匹配,皮爾遜相關性為0.97(圖2d)。
此外,圖2e顯示,天然Cas9、祖先序列重建和48個生成蛋白的靶上和脫靶的編輯效率。圖2f展示自然Cas9、祖先序列重建,以及生成蛋白在靶向編輯效率和特異性方面的對比。
生成的基因編輯器,在人類細胞中發揮作用
然後,研究者進一步將關註范圍縮小到CRISPR-Cas9系統,並在CRISPR-Cas圖譜中的238,917個Cas9蛋白上,訓練蛋白質語言模型。
使用這些模型,研究者生成可與SpCas9互操作的Cas9樣蛋白。也就是說,它們與基因組的相同部分(PAM)結合,並與相同的sgRNA相容,因此,它們可用於相同的應用。
研究者選擇其中48個生成的序列,用於在人類細胞中進行嚴格的功能表征。
最熱門的OpenCRISPR-1,在靶向位點的活性與SpCas9相當(OpenCRISPR-1的編輯率為55.7%,SpCas9的編輯率為48.3%),但令人驚訝的是,在脫靶位點的編輯減少95%(OpenCRISPR-1的編輯率為0.32%,SpCas9為6.1%)。
此外,作為一種非常新的蛋白質,OpenCRISPR-1與SpCas9相距403個突變,與 CRISPR-Cas圖譜中的任何天然蛋白質相距182個突變。
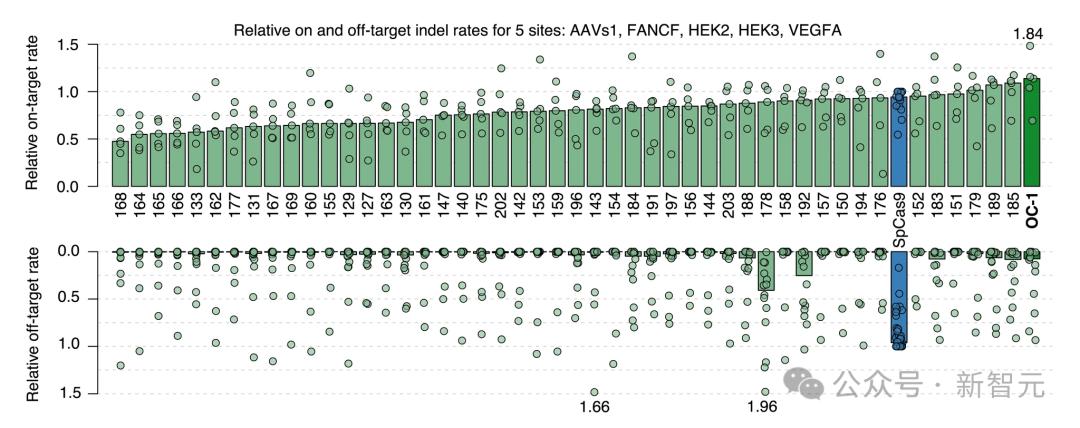
多種生成的核酸酶(綠色),包括OpenCRISPR-1(深綠色),具有與SpCas9(藍色)相當或更高的靶向活性,但脫靶活性要低得多
研究者們還發現,當與脫氨酶配對時,OpenCRISPR-1和SpCas9在精確編輯靶基因組中的單個堿基時,具有相似的活性和特異性。
他們還能保持堿基編輯活性,同時通過用由另一種Profluent訓練的蛋白質語言模型生成的脫氨酶,來提高特異性。
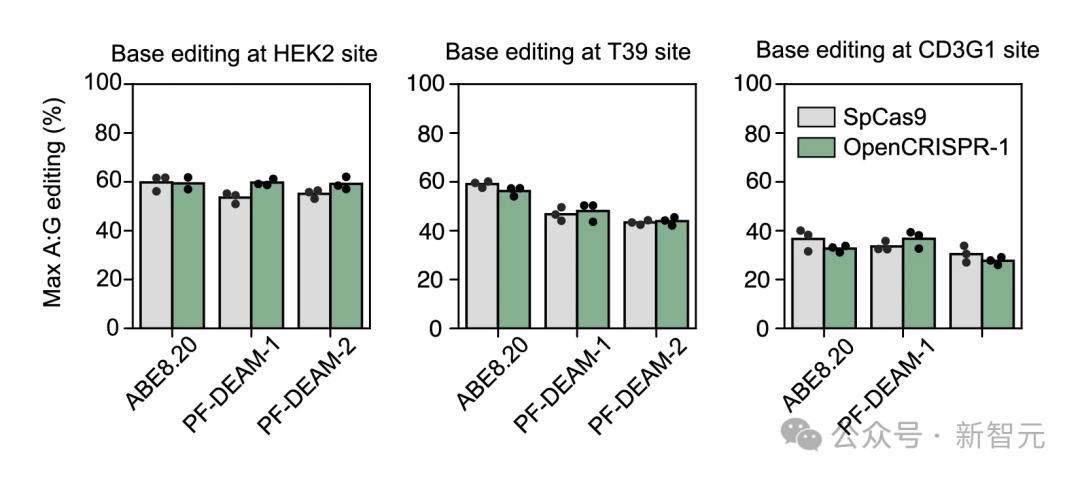
使用ABE8.20(一種高活性工程脫氨酶)以及生成的脫氨酶PF-DEAM-1和PF-DEAM-2進行堿基編輯時,OpenCRISPR-1的功能與SpCas9非常相似
最後,為進一步優化所生成的核酸酶的活性,研究者還訓練一個模型來為任何給定的Cas9樣蛋白生成相容的sgRNA。
與SpCas9的sgRNA相比,這些生成的sgRNA可以提高所測試的五種蛋白質中四種產生的核酸酶的活性。
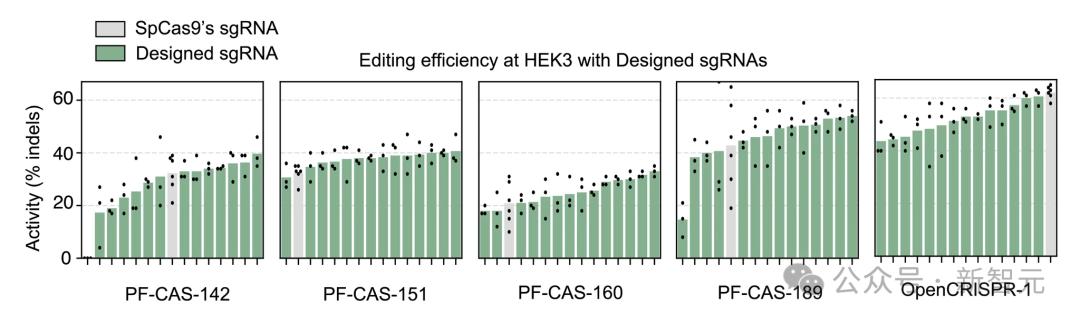
對於測試的5種生成的核酸酶中的4種,使用模型生成的sgRNA提高編輯效率
AI,正在改善醫療保健
現在,全世界都有很多項目,在用AI技術改善醫療保健。
比如,華盛頓大學的科學傢們正在用ChatGPT和Midjourney背後的方法來,創造全新的蛋白質,並且正在努力加速新疫苗和藥物的開發。
如今大火的許多生成式AI,背後都是由神經網絡驅動的。通過分析大量數據,神經網絡就習得某些技能。
比如,Midjourney以神經網絡為基礎,分析數百萬張數字圖像,以及描述每張圖像的標題。這樣,系統就學會識別圖像和文字之間的聯系,可以畫出“犀牛從金門大橋上跳下來”這樣的畫。

Profluent的技術,也是由一個類似的AI模型驅動的。
這個模型從氨基酸和核酸序列中學習,正是這些化合物,定義科學傢用來編輯基因的微觀生物學機制。
本質而言,它就是分析從自然界中提取的CRISPR基因編輯器的行為,學習如何生成全新的基因編輯器。
Profluent的CEO Ali Madani介紹道,這些AI模型都是從序列中學習的,無論是字符、單詞、計算機代碼,還是氨基酸的序列。

Madani先生在加州伯克利Profluent實驗室內,此前他曾在軟件巨頭Salesforce的人工智能實驗室工作
人類編輯基因,還會有多遠
目前,Profluent尚未對這些合成基因編輯器進行臨床試驗,因此尚不清楚它們是否能與CRISPR的性能相媲美,甚至超過CRISPR。
但他們的研究表明,AI模型可以產生能夠編輯人類基因組的東西。
盡管如此,這項成果還不太可能在短期內影響醫療保健。

UC伯克利創新基因組學研究所的基因編輯先驅兼科學主任費Fyodor Urnov表示,科學傢們並不缺乏天然存在的基因編輯器,用來對抗疾病。
真正的瓶頸在於,這項編輯器在用於臨床治療之前,還會因安全性、制造、監管審查產生極高的成本。
但是,隨著學習越來越多的數據,生成式AI系統的潛力不可小覷。
如果Profluent的技術繼續改進,終有一天,科學傢們可以用更精確的方式編輯基因。
到那時,我們可能身處這樣一個世界——許多藥物和治療方法,都能快速為個人量身定制。這是今天的人們所不敢想的。
“我夢想著這樣一個世界,我們可以在幾周內按需提供CRISPR,” Urnov博士說。

還有一個重大的問題就是,CRIPSR有風險嗎?
長期以來,科學傢們一直在警告:不要使用CRISPR進行人類增強!
因為,這是一項相對較新的技術,很可能會產生不良的副作用,比如引發癌癥。而且還有些人會用於非道德的用途,比如轉基因人類胚胎。
合成基因編輯器,也面臨著這項問題。而如今,科學傢們已經掌握編輯胚胎所需的一切技術。
但Fraser博士表示,如果真的有人想用它們做壞事,也隻會使用現有的東西,而非AI創建的編輯器。